Jak powstają nowotwory?
Nowotwory zawsze rozwijają się jako wynik mutacji, tj. nagle wywołanych zmian w naszych genach. Geny to komplet instrukcji, których prawidłowe działanie zapewnia właściwe funkcjonowanie całego naszego ciała. Są zapisane w ledwie widocznym pod mikroskopem elektronowym materiale – DNA – który dziedziczymy po połowie od każdego z naszych rodziców.
Pojawienie się uszkodzenia genetycznego powoduje utratę kontroli organizmu nad działaniem komórki, prowadząc do uzyskania przez nią pewnej autonomii i w konsekwencji do niekontrolowanych podziałów. Prawidłowe komórki naszego ciała dzielą się i rosną jedynie w sposób w pełni włączany i wyłączany przez organizm. Chore – nowotworowe – komórki dzielą się (czyli namnażają) szybciej niż zdrowe, czego skutkiem jest powstawanie guza nowotworowego.
Większość nowotworów, zwanych nowotworami sporadycznymi, jest powodowanych przez różne czynniki środowiskowe, które wywołują mutacje w DNA pojedynczych komórek, prowadząc do ich niekontrolowanych podziałów. Tak powstałe mutacje można wykryć jedynie w materiale pochodzącym z nowotworu.
Odmiennie, nowotwory dziedziczne (rodzinne) są indukowane zmianami genetycznymi, które dziedziczymy od rodziców. Takie zmiany są obecne w DNA niemal wszystkich komórek naszego organizmu i przede wszystkim dotyczą genów, których zadaniem jest chronienie nas przed uszkadzającym działaniem środowiska. Mówimy, że ich obecność predysponuje do zachorowania na określony typu nowotworu, nie wiąże się bowiem z pewnością, że dojdzie do rozwinięcia choroby, ale oznacza znacząco zwiększone prawdopodobieństwo jej wystąpienia.
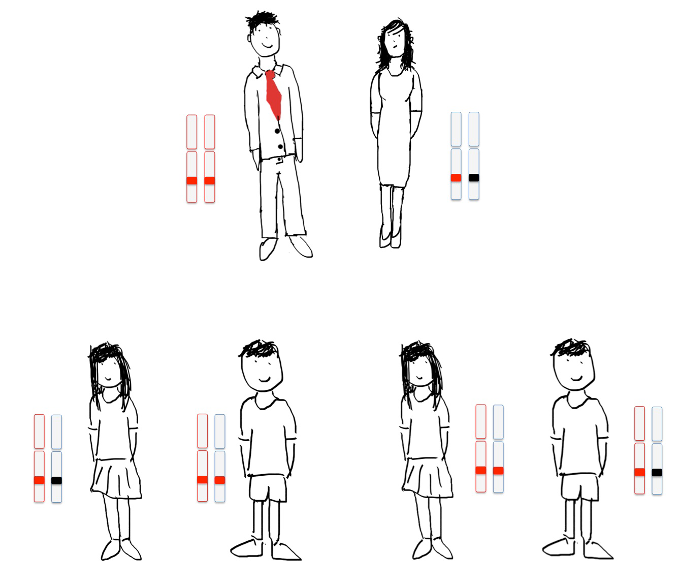
Ryc. 1 Każdy z nas ma po 2 kopie genów. Jedną kopię genu dziedziczymy od matki, drugą od ojca. Ponieważ DNA dziecka pochodzi w połowie od każdego z rodziców, dziecko pacjenta z uszkodzeniem genetycznym, warunkującym zwiększone ryzyko raka, ma 50% ryzyko odziedziczenia wadliwego genu (zaznaczonego kolorem czarnym). Dziedziczenie to nie jest zależne od płci.
Co się dzieje gdy odziedziczymy chorobotwórczą mutację?
Większość nowotworów występuje sporadycznie, ale 10-20% wszystkich zachorowań stanowią raki dziedziczne. Co istotne, pacjentki będące nosicielkami mutacji predysponującej do jednego typu nowotworu, np. raka jajnika, mają zwiększone ryzyko zachorowania na inne nowotwory, w tym raka piersi, trzustki i czerniaka. Pacjentki z dziedzicznym rakiem jelita grubego mają zwiększone ryzyko zachorowania na raka żołądka, trzustki, endometrium i jajnika. Można więc powiedzieć, że chorobotwórcza mutacja predysponuje do całego zespołu powiązanych chorób. Dodatkowo, obciążeni pacjenci chorują na nowotwory znacznie wcześniej, niż spodziewamy się tego przy nowotworach sporadycznych – ryzyko zachorowania rośnie znacząco już w 30-35 roku życia. Zdobycie informacji na temat posiadania wadliwego genu umożliwia zatem zadbanie o bardziej skuteczną profilaktykę – prowadzenie częstszych i bardziej ukierunkowanych badań pozwalających na wykrycie nowotworów we wczesnych stadiach. Pozwala także lepiej zaopiekować się całymi rodzinami.
Czy istnieje coś takiego jak dziedzicznie uwarunkowane ryzyko zachorowania na nowotwory kobiece?
Zespoły chorobowe, w których występują nowotwory piersi, jajników, jajowodów i macicy mogą być powodowane mutacjami w licznych genach. W raku piersi i jajnika najczęściej identyfikowane mutacje dotyczą genów BRCA1 i BRCA2 oraz PALB2, które odpowiadają za 20-25% przypadków rodzinnego raka piersi i 15% przypadków raka jajnika. Dziedziczne nowotwory endometrium są najczęściej wynikiem mutacji genów PTEN bądź EPCAM, MLH1, MSH2, MSH6, PMS2 których uszkodzenia powodują zespół chorób nazwany Zespołem Lyncha.
Pamiętajmy jednak! Pewne zmiany genetyczne predysponują w sposób szczególny do nowotworów „kobiecych” ale to nie oznacza, że obciążeni nimi mężczyźni nie są zagrożeni chorobą. Przy uszkodzeniu genów związanych z dziedzicznym rakiem piersi i jajnika najczęściej spodziewamy się u mężczyzn wzrostu ryzyka zachorowania na raka piersi i prostaty, przy zespole Lyncha – mężczyźni mogą chorować na nowotwory przewodu pokarmowego. Nie jest prawdą, że nowotwory dziedziczą się linią kobiecą lub linią męską.
Jak zmienia się ryzyko zachorowania, gdy odziedziczyliśmy chorobotwórczą mutację? I jak te geny badać?
Dziedziczne raki piersi i jajnika oraz macicy są powodowane mutacjami w licznych genach. Żeby zrozumieć w jaki sposób taka mutacja wpływa na ryzyko zachorowania, należy odnieść się do pojęcia ryzyka populacyjnego – tj takiego jakie ma każdy z nas, nie obciążony mutacją. Statystyki wskazują, że na raka piersi zachoruje mniej więcej co 8-9 kobieta (ryzyko zachorowania wynosi 12%), na raka jajnika co 50 kobieta (ryzyko nie przekracza 2%), na raka endometrium co 36 kobieta (ryzyko wynosi ok 3%). Najważniejsze geny związane z rakami jajnika oraz macicy i ich wpływ na kształtowanie ryzyka także innych nowotworów wymieniono pod tekstem.
Dlaczego mówienie o tych wszystkich genach jest ważne? Dlatego, że aby poznać swoje obciążenie chorobą nowotworową, musimy zadbać by przebadane zostały wszystkie geny, których uszkodzenia mogą ją powodować. Niestety w Polsce często wykonuje się małe, wybiórcze badania genetyczne, w których albo zagląda się w 1-2 geny, albo, jeszcze częściej, w wybrane ich punkty. Wyobraźmy sobie geny jako długie sznurki, w których każdym węzełku może się pojawić uszkodzenie. Tradycyjnie wykonywane badania analizują tylko wybrane lokalizacje – np. 7 potencjalnie uszkodzonych miejsc w genie BRCA1, podczas gdy aktualnie znamy 4212 mutacje mogące powodować zwiększone ryzyko nowotworu. Metoda analizy genetycznej, która zapewnia zajrzenie we wszystkie węzełki genu to sekwencjonowanie nowej generacji (NGS). Warto się upewnić, że taką właśnie metodę zastosowano wykonując nasze badanie. Czasem konieczne będzie przeprowadzenie analizy uzupełniającej metodą MLPA; jej celem jest znalezienie w genach rozległych dziur (delecji), których obecność może umknąć badaniu NGS.
Podkreślmy także, że wiedza o obciążeniu genetycznym ważna jest także z perspektywy pacjentki, która już zachorowała na nowotwór – pomaga ustawić właściwe leczenie, w tym leczenie celowane.
Geny, których uszkodzenia powodują nowotwory jajnika i endometrium:
ATM – 2-3% ryzyko raka jajnika
20-40% ryzyko raka piersi, 5-10% ryzyko raka trzustki
BRCA1- 39-58% ryzyko raka jajnika
> 60% ryzyko raka piersi u kobiet
<2% ryzyko raka piersi u mężczyzn
5% ryzyko raka trzustki
7-26 % ryzyko raka prostaty
BRCA2 – 13-29% ryzyko raka jajnika
> 60% ryzyko raka piersi u kobiet
2-7% ryzyko raka piersi u mężczyzn
5-10% ryzyko raka trzustki
19-60 % ryzyko raka prostaty
BRIP1 – 5-15% ryzyko raka jajnika
PALB2 3-5% ryzyko raka jajnika
41-60% ryzyko raka piersi
5-10% ryzyko raka endometrium
RAD51C i RAD51D – 10-15% ryzyko raka jajnika
20-40% ryzyko raka piersi
PTEN – 25-30% ryzyko raka endometrium
40-60% ryzyko raka piersi
Zwiększone ryzyko nowotworów nerki, tarczycy, jelita grubego oraz czerniaka.
MLH1 – 4-20% ryzyko raka jajnika
34-54% ryzyko raka endometrium
5-10% ryzyko raka trzustki
46-61% ryzyko raka jelita grubego
Zwiększone ryzyko innych nowotworów przewodu pokarmowego oraz nerki i moczowodów, pęcherza moczowego.
MSH2/EPCAM – 8-38% ryzyko raka jajnika
21-57% ryzyko raka endometrium
Zwiększone ryzyko innych nowotworów przewodu pokarmowego oraz nerki i moczowodów, pęcherza moczowego.
MSH6 – 1-13% ryzyko raka jajnika
16-49% ryzyko raka endometrium
Zwiększone ryzyko innych nowotworów przewodu pokarmowego oraz nerki i moczowodów, pęcherza moczowego.
PMS2 – 1-3% ryzyko raka jajnika
13-26% ryzyko raka endometrium
Zwiększone ryzyko innych nowotworów przewodu pokarmowego oraz nerki i moczowodów, pęcherza moczowego.
AUTOR: Dr hab. n. med. Anna Wójcicka, Fundacja ”Wiedzieć Więcej”



